Diagnostik und Therapie des Lipödems
Interessengebiete: Allgemeinmedizin und Innere Medizin, Haut- und Geschlechtskrankheiten
Beim Lipödem handelt es sich um eine schmerzhafte symmetrische Fettverteilungsstörung mit Disproportion der Extremitäten zum Stamm. Durch die Lipohypertrophie oder Lipohyperplasie an den Oberschenkeln kann es zu Gangstörungen und Wunden kommen. Das Lipödem betrifft fast ausschließlich Frauen. Die Erkrankung verläuft chronisch, manchmal auch progredient. Erste Symptome manifestieren sich häufig in Phasen hormoneller Umstellungen wie in der Pubertät, Schwangerschaft oder Menopause.
Diese CME gibt einen Überblick zur Pathogenese, Diagnostik und Therapie beim Lipödem auf Basis der aktuellen S2k-Leitlinie Lipödem der Deutschen Gesellschaft für Phlebologie und Lymphologie.
Kursinhalt
Inhaltsverzeichnis
Einleitung
Seit der Erstbeschreibung von Alan und Hines 1940 wird versucht, das Krankheitsbild, unter dem fast nur Frauen leiden, einzuordnen, die Ursachen zu finden und eine zielgerichtete Therapie anzubieten. Nach aktueller Definition handelt es sich um eine schmerzhafte symmetrische Fettverteilungsstörung mit Disproportion der Extremitäten zum Stamm unter Aussparung der Hände und Füße. Volumenvermehrungen ohne Schmerzen werden entgegen häufiger früherer Darstellung nicht als Lipödem bezeichnet. Zur schwierigen Abgrenzung zur Adipositas in Kombination mit anderen schmerzverursachenden Krankheiten wird klargestellt, dass das Lipödem zwar oft von Adipositas begleitet wird, sie aber nicht verursacht [1, 2].
Die in der früheren Leitlinie beschriebene Hämatomneigung wurde ebenso wenig wie die Knotenbildung im Fettgewebe in Studien bewiesen.
Epidemiologie
Belastbare epidemiologische Daten zum Lipödem gibt es nicht. Selbst die aktuelle Leitlinie von 2024 konstatiert: „Studien zur Epidemiologie, die den aktuellen Diagnosekriterien standhalten, existieren nicht. … Zitiert werden in nahezu allen Veröffentlichungen Studien oder Arbeiten, die älter als 10 Jahre sind“ [3].
Fast man diese vergleichsweise alten Daten zusammen, ergibt sich folgendes Bild:
Die Schätzung von bis zu 11 % der am häufigsten zitierten Arbeit aus dem Lehrbuch von Földi [4] wurde in den Auflagen ab 2012 nicht mehr genannt und 2019 widerrufen. Aufgrund der verschiedenen Definitionen und Untersuchungskollektive sind keine validen Zahlenangaben möglich.
Pathophysiologie
Pathogenese des Lipödems
Die genaue Ursache des Lipödems ist nicht vollständig geklärt, aber es wird angenommen, dass eine Kombination aus genetischen, hormonellen und entzündlichen Faktoren eine Rolle spielt. Es existieren verschiedene Hypothesen zum Pathomechanismus [5] (Abb. 1). Bislang wird diskutiert, ob beim Lipödem eine Hyperplasie (Zunahme der Zellzahl) oder eine Hypertrophie (Zunahme der Zellmasse) der subkutanen Fettzellen vorliegt [6, 7]. Vor allem die initialen Differenzierungsschritte der Adipogenese scheinen betroffen [8-10].
Genetische Prädisposition: Aufgrund der familiären Häufung wird eine genetische Prädisposition angenommen [11].
Hormonvermittelte Störung: Der Erkrankungsbeginn fällt in der Regel mit Phasen hormoneller Veränderungen zusammen, daher wird eine Östrogen-vermittelte Störung [12] vermutet. Die phänotypischen Veränderungen und Krankheitsschübe im Verlauf des Lipödems korrelieren mit Schwangerschaft, Pubertät und Menopause [24]. Östrogen könnte die Hyperproliferation der Adipozyten stimulieren und durch „Insulin-like growth factor 1“ (IGF-1) ihre Zellexpansion und Differenzierung fördern [13].
Niedrigschwellige Entzündung: Der Schmerz ist das Leitsymptom des Lipödems. Er kann in jedem Lipödemstadium auftreten und korreliert nicht mit der Schwere der Fettverteilungsstörung oder dem Body-Mass-Index (BMI). Als Schmerzursache wird eine inflammatorisch bedingte Dysregulation von sensorischen Nervenfasern vermutet. Als auslösende Faktoren der Schmerzentstehung werden Östrogene, überstarke sympathische Nervenaktivität und eine Hyperalgesie diskutiert [14].
Krankheitsverlauf
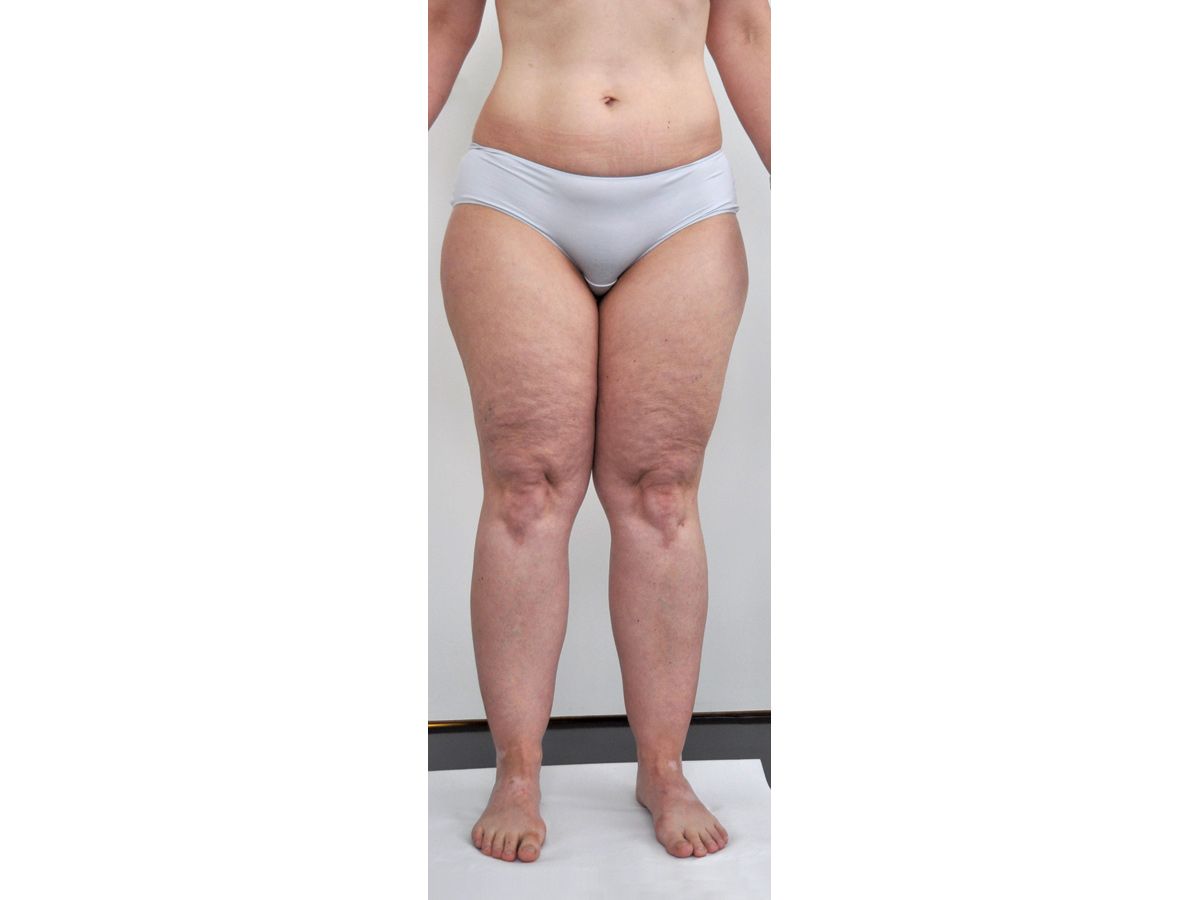
Im Krankheitsverlauf kommt es zu einem verstärkten Schmerz und Fettzunahme, danach kann es vermehrt zu Folgeerscheinungen des Lipödems kommen. Die Progredienz ist sehr verschieden, nicht immer vorhanden und korreliert oft mit allgemeiner Gewichtzunahme, bei einer hohen Koinzidenz mit Adipositas. Die Volumenzunahme infolge Vermehrung subkutanen Fettgewebes an den Extremitäten [Abb. 2] kann diskret sein, aber auch bis zu überhängendem Gewebe (Wammen) an Knien, supramalleolär und über den Ellenbogen reichen. Als Folgen können mechanische Irritationen und Hautmazerationen entstehen. Wammen an den Oberschenkelinnenseiten und Kniegelenken resultieren darüber hinaus in Störungen des Gangbildes mit sekundären Arthrosen [15].
Die Erkrankung geht häufig einher mit psychischer Beeinträchtigung und reduziertem Selbstwertgefühl, da das Aussehen nicht dem gängigen Schönheitsideal entspricht [15].
Diagnostik
Die diagnostischen Kriterien gehen auf die Erstbeschreibung 1940 zurück und wurden seitdem mehrfach überarbeitet [5, 16, 17].
Klinisches Bild
Die Diagnose Lipödem soll laut aktueller Leitlinie auch weiterhin klinisch gestellt werden [3]. Hintergrund dafür ist, dass keine richtungsweisenden apparativen und laborchemischen Verfahren vorhanden sind, die die Diagnose Lipödem beweisen können.
Die Basisdiagnostik, die aus Anamnese, Inspektion und Palpation besteht, sollte besonders die häufigen Symptome berücksichtigen [3, 15]:
- bilateral symmetrische disproportionale Fettgewebsvermehrung der Arme und Beine
- Druck- und Berührungsschmerz
Die bisher verwendete Stadieneinteilung beschreibt nicht den Schweregrad der Erkrankung und sollte dafür nicht mehr verwendet werden.
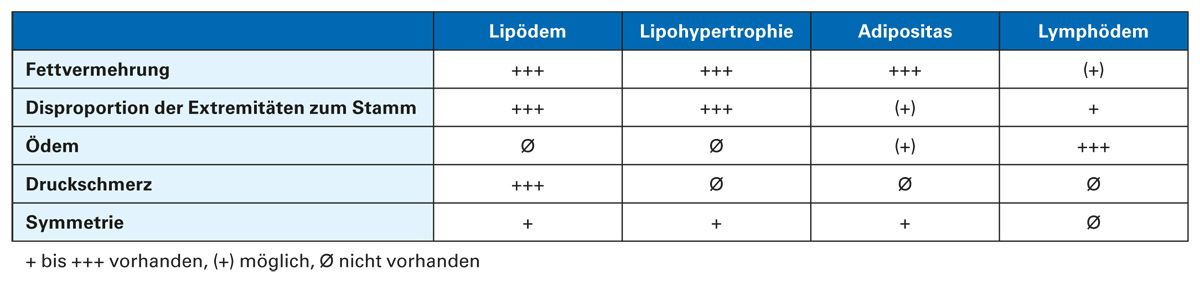
Differenzialdiagnosen
Die wichtigsten Differenzialdiagnosen sind die zentrale Adipositas und das Lymphödem [18] (Tab. 1). Beide Erkrankungen können bei Patientinnen mit einem Lipödem auftreten und sind nach bisherigen Erkenntnissen nicht Folge des Lipödems. Das Lipödem an sich verursacht kein Lymphödem, eine begleitende Adipositas kann jedoch zur Bildung eines Lymphödems führen. Das Vorliegen der Leitsymptome Schmerzen und Spannungsgefühl deuten auch bei bestehender Adipositas auf ein Lipödem hin. Häufig assoziierte psychische Begleiterkrankungen sollten routinemäßig erfragt werden, um gegebenenfalls frühzeitig eine notwendige Therapie zu beginnen.
Labordaten, um die Diagnose des Lipödems weiter zu spezifizieren, existieren nicht. Entsprechend formuliert die Leitlinie: Laborparameter können zum Ausschluss von Differenzialdiagnosen genutzt werden, sind aber nicht geeignet das Lipödem zu beweisen [3].
Auch apparative Verfahren dienen ausschließlich zur differenzialdiagnostischen Abgrenzung anderer Krankheitsbilder und konnten sich bislang in der Routinediagnostik des Lipödems nicht etablieren [15, 16]. Laborchemisch sollten Nieren- und Leberfunktionsstörungen, (subklinische) Hypothyreosen sowie pathologische Lipidprofile und Insulinresistenzen ausgeschlossen werden.
Standardisierte anthropometrische Messungen sollten in der klinischen Routine insbesondere zur Beurteilung des Spontanverlaufs und zur Beurteilung des Therapieansprechens erfolgen: Körpergewicht, Body-Mass-Index (BMI), Waist-to-Hip-Ratio (WHR), Waist-to-Height-Ratio (WHtR) sowie Umfangs- und Volumenmessungen der Extremitäten [3]. Ergänzend kann ein Assessment zur Schmerzwahrnehmung erfolgen, zum Beispiel anhand der visuellen Analogskala (VAS). Zudem sollte der tägliche Aktivitätsindex dokumentiert werden, zum Beispiel per Schrittzähler.
Therapieoptionen
Die Therapie des Lipödems hat als wesentliche Ziele die Schmerzreduktion, die Verbesserung der funktionalen Einschränkungen und die Prävention der Krankheitsprogression [39]. Es gibt keine medikamentöse Therapie. Diuretika sollen laut Leitlinie nicht zur Behandlung des Lipödems eingesetzt werden [3].
Zum Einsatz von Schmerzmitteln sagt die Leitlinie: In der initialen Therapiephase oder bei besonderer Befundverschlechterung kann eine medikamentöse Schmerztherapie in Betracht gezogen werden. Allerdings ist diese nach Expertenerfahrungen beim Lipödem in der Regel wirkungslos. Patientinnen sollten wissen, dass die Therapie primär auf eine Beschwerdelinderung zielt, nicht auf eine Formveränderung der Extremitäten [15].
Kompressionstherapie
Der Einsatz der Kompressionstherapie beim Lipödem gehört zur Basistherapie und die
Leitlinie formuliert folgende Empfehlungen [3]:
- ei diagnostiziertem Lipödem soll die Kompressionstherapie zur Schmerzreduktion an den betroffenen Extremitäten eingesetzt werden (Empfehlung 4.1).
- Die Kompressionstherapie beim Lipödem kann initial mit medizinischen Kompressionsstrümpfen (MKS), Kompressionsverbänden (KV) und medizinisch adaptiven Kompressionssystemen (MAK) erfolgen. In der Langzeitbehandlung sollten im Routinefall MKS bevorzugt werden (Empfehlung 4.2).
- Die Kompressionstherapie soll beim Lipödem auf die Reduktion von Schmerzen und anderen subjektiven Symptomen ausgerichtet sein (Empfehlung 4.3).
- Es soll den Patientinnen vermittelt werden, dass die Kompression nicht zur Reduktion des Fettgewebes geeignet ist (Empfehlung 4.4).
Aufgrund der subjektiven Schmerz- und Beschwerdesymptomatik ist eine patientenindividuelle und ganzheitliche Therapie erforderlich. Bei der Auswahl und der Verordnung der Kompressionsmaterialien soll neben dem erforderlichen Druck auch das individuell am besten geeignete Material berücksichtigt werden, da die Wirkung der Kompressionsversorgung sowohl vom Druck als auch von den Materialeigenschaften abhängt.
Eine gemeinsame Entscheidung von Patientin, Arzt, Therapeut und Versorger kann zur Verbesserung der Adhärenz und damit auch der Wirksamkeit beitragen [3]. Die Leitlinie gibt differenzierte Empfehlungen [3]:
- Das Lipödem kann grundsätzlich mit rund- oder flachgestrickten MKS behandelt werden. Bei großen Umfangsänderungen an einer Extremität bzw. konisch geformten Extremitäten sowie bei vertieften Gewebefalten soll eine flachgestrickte Qualität verordnet werden, da bei diesen anatomischen Verhältnissen rundgestricktes Material ungeeignet ist (Empfehlung 4.7).
- Aufgrund der Strickart weisen flachgestrickte MKS in der Regel eine höhere Stiffness, aber auch eine höhere Biegesteifigkeit auf. Diese Eigenschaften sollten bei der Versorgung von Patientinnen mit Lipödemen sowie bei begleitender Adipositas genutzt werden. Die höhere Biegesteifigkeit überbrückt tiefere Gewebefalten besser, ohne durch „Hineinrutschen“ zu Abschnürungen zu führen (Empfehlung 4.8).
- Strumpfart und Stärke des erforderlichen Andrucks, d. h. die Kompressionsklasse (KKL), sollen an die Lokalisation, den klinischen Befund und die Schwere der Beschwerden und Veränderungen angepasst werden. Eine starre Zuordnung einer KKL zur Diagnose Lipödem soll nicht erfolgen, da das Ziel der Kompressionstherapie die Besserung der subjektiven Symptome, insbesondere des Schmerzes, ist (Empfehlung 4.9).
- Es soll immer die niedrigste KKL bevorzugt werden, die zu einer ausreichenden Symptomlinderung führt. Dies unterstützt die Adhärenz mit der Kompressionstherapie (Empfehlung 4.10).
Weitere konservative Therapiekomponenten
Die klassischen konservativen Therapiekomponenten können weiterhin umfassen:
- Physio- beziehungsweise Bewegungstherapie
- psychosoziale Therapie
Die Leitlinie hält dazu fest [3]: Falls die Kompression in Einzelfällen nicht anwendbar ist oder allein nicht zu einer Schmerzreduktion führt, kann das Leitsymptom Schmerz mittels zusätzlicher Lymphdrainage in Kombination mit weiteren Therapietechniken behandelt werden (Empfehlung 7.1). Die manuelle Lymphdrainage zielt hierbei nicht auf eine Volumenreduktion, sondern auf die Modulation der C-Fasern ab.
Da Bewegung in Kompression bzw. ein Trainingsprogramm ein wichtiges Element in der Schmerzreduktion darstellt, soll sie in das therapeutische Gesamtkonzept einbezogen werden (Empfehlung 7.2). Zur alleinigen Anwendung der Therapietechnik Manuelle Lymphdrainage (MLD) schreibt die Leitlinie: „… findet sich beim Lipödem keine Evidenzlage. Vielmehr wurde diese in verschiedenen Kombinationsformen zu anderweitigen Therapieformen untersucht. Dennoch sei darauf hingewiesen, dass für die Manuelle Lymphdrainage sowohl eine sympathikolytische Wirkung als auch eine Erhöhung der Schmerztoleranz sowie eine Erhöhung der Schmerzschwelle nachgewiesen sind.“
Weitere in der Leitlinie [3] vorgestellte und diskutierte Verfahren sind u.a. die Vibrationsplatte zur Anhebung der Druckschmerzschwelle und eine Schmerzreduktion über ein Beinmuskeltraining. Empfehlung 7.3 lautet: Die Vibrationsplatte kann mit dem Ziel der Erhöhung der Druckschmerzschwelle eingesetzt werden.
Die Komplexe Physikalische Entstauungstherapie sollte bei Lipödemen mit additiven Ödemen anderer Genese eingesetzt werden (Empfehlung 7.4). Die additive Durchführung von Aquasport (z. B. Aquacyling) kann einen positiven Einfluss aufweisen (Empfehlung 7.5). Die Manuelle Lymphdrainage in Kombination mit weiteren Therapietechniken sollte zur Verbesserung der Lebensqualität (QoL) in Betracht gezogen werden (Empfehlung 7.6) [3]. Zu beachten sind dabei in Deutschland die aktuellen Heilmittelrichtlinien.
Eine signifikante Verbesserung einer vorliegenden Depression durch körperliche Aktivität konnte mehrfach gezeigt werden. Studien lassen eine Korrelation interozeptiver
Signalgebung sowie Angststörungen und Depressionen wahrscheinlich erscheinen [20, 21]. Studien an Lipödempatientinnen fehlen.
Lebensstilanpassungen und Selbstmanagement
Das Lipödem ist assoziiert mit einem erhöhten Risiko für Übergewicht und Adipositas, was wiederum die Symptomatik der Erkrankung verstärken kann [22, 23]. Der BMI soll nicht mehr alleine zur Abgrenzung zwischen Lipödem und Adipositas verwendet werden. Die Leitlinie empfiehlt daher: Zur Erstdokumentation und Verlaufskontrolle sollen zumindest die biometrischen Werte Körpergewicht, Körpergröße sowie Taillen- und Hüftumfang erhoben werden [3]. Die Therapie von Übergewicht und Adipositas soll in das Gesamtkonzept der Therapie des Lipödems einbezogen werden.
Gute Wirkungen auf Körpergewicht und Wohlbefinden wurden beobachtet u. a. für die niedrigkalorische, ketogene Diät [24], eine modifizierte mediterrane ketogene Diät mit Carboxytherapie [25] und eine kohlenhydratarme, fettreiche Diät [26].
Auch durch körperliche Aktivität können mentale und physische Gesundheit positiv beeinflusst werden [27], sie soll daher in das therapeutische Gesamtkonzept einbezogen werden. Die Bewegungstherapie sollte dabei an die individuellen Möglichkeiten angepasst werden. Grundsätzlich zu empfehlen sind Sportarten mit Geh- oder Laufbewegungen unter Aktivierung der Wadenmuskelpumpe.
Effektives Selbstmanagement ist ein wichtiger Bestandteil der Gesundheitskompetenz. Sie soll gefördert und die Patientin zur aktiven Rolle ermutigt werden. Problemlösestrategien und konkrete individuelle Therapieziele sollen gemeinsam erarbeitet werden und so die Erhöhung der Selbstwirksamkeit gefördert werden (Empfehlung 9.1). Dazu gehören Teilkompetenzen wie zum Beispiel Motivation, Zielsetzung, Planung, Zeitmanagement, Organisation, Erfolgskontrolle oder Feedback [28].
Selbstmanagement sollte durch geeignete Maßnahmen von den Behandlern unterstützt werden, die Verantwortung bei der Patientin bleiben. Die Behandler sollten Erfolge positiv verstärken. Konfrontatives Verhalten soll vermieden werden (Empfehlung 9.2).
Das Vermitteln wissenschaftlich fundierter Informationen über die Erkrankung im Rahmen der Patientenschulung ist auch beim Lipödem essenziell. Nur auf der Basis valider Informationen kann ein gelingendes Selbstmanagement aufgebaut werden. Fehlinformationen verhindern ein erfolgreiches Selbstmanagement und können zu einer Verschlechterung des Erkrankungsverlaufs führen [29, 30].
Vorab ist zu klären, inwieweit die Patientin zum Selbstmanagement fähig ist. Falls eine Einschränkung besteht, ist eine Unterstützung durch andere zu hinterfragen und zu organisieren. Diese Patientinnen benötigen dann phasenweise eine engmaschigere Unterstützung oder Überweisung an weitere Fachgruppen wie z. B. Psychotherapeuten [3].
Spezielle Selbstmanagement-Programme können ein erfolgreiches Selbstmanagement bei Patientinnen mit chronischen Erkrankungen unterstützen. Gesundheitsexperten fördern Selbstmanagement durch verhaltensorientierte Beratung und motivierende Gesprächsführung auf Augenhöhe [3, 31]. Ziel soll sein, dass die Patientin zur Expertin für ihre eigene Erkrankung wird.
- Kompressionstherapie: täglich
- Physiotherapie / Gymnastik: 1- bis 2-mal pro Woche und tägliche Übungen für zu
Hause - Hautpflege: täglich
Operative Methoden
Als operative Methode der Wahl zur nachhaltigen Reduktion des betroffenen Unterhautfettgewebes des Lipödems an Beinen und Armen soll laut Leitlinie die Liposuktion eingesetzt werden (Empfehlung 12.1) [3]. Das Verfahren gilt als effektiv – vor allem, was Schmerzlinderung, Mobilitätsverbesserung und Erhöhung der Lebensqualität betrifft [32-34]. Die lymphatische Funktion sollte nicht beeinträchtigt werden. Die absolute Schmerzreduktion wird beeinflusst durch den präoperativen Schmerzwert, das Lipödemausmaß, den Behandlungszeitraum und das Alter der Patientinnen [35].
Unmittelbar nach Liposuktion sollte eine komplexe physikalische Entstauungstherapie durchgeführt werden und die Patientinnen sollen weiter abhängig von der Beschwerdesymptomatik konservativ behandelt werden.
Fazit
Die Diagnose Lipödem ist bei fehlenden Laborparametern oder sonstigen apparativen Untersuchungsmethoden klinisch zu stellen und ist auf die schmerzhafte symmetrische
Fettgewebszunahme an Armen und Beinen eingegrenzt. Andere Körperteile sind nicht betroffen, können aber im Rahmen begleitender Adipositas auch vermehrtes Volumen
aufweisen.
Zur Ursache zeigen die Studien unterschiedliche Ergebnisse und verdeutlichen damit den weiterhin hohen Forschungsbedarf. Da sich erste Symptome häufig in Phasen hormoneller Umstellungen (Pubertät, Schwangerschaft, Menopause) manifestieren, wird ein Zusammenhang angenommen.
Therapeutisch stehen momentan konservative und operative Verfahren zur Verfügung, die sich häufig ergänzen und individuell ausgewählt werden sollten.
Hinweis:
Aus Gründen der besseren Lesbarkeit wird auf die gleichzeitige Verwendung der Sprachformen männlich, weiblich und divers
(m/w/d) verzichtet. Entsprechende Begriffe gelten im Sinne der Gleichbehandlung grundsätzlich für alle Geschlechter. Die
verkürzte Sprachform beinhaltet keine Wertung.
Literatur
- Wollina U (2019) Lipedema – an update. Dermatol Ther 32(2): e12805
- Shavit E et al (2018) Lipoedema is not lymphoedema: A review of current literature. Int Wound J 15(6): 921–928
- S2k-Leitlinie Lipödem. Deutsche Gesellschaft für Phlebologie und Lymphologie e.V.: S2K-Lipödem, 5.0, 2024, https://register.awmf.org/de/leitlinien/detail/037-012 (abgerufen am: 29.07.2024)
- Földi M et al (2003). Textbook of Lymphology. Elsevier, New York
- Wollina U (2024) Klinik und Therapie des Lipödems. CardioVasc 24(3): 39-43
- Suga H et al (2009) Adipose tissue remodeling in lipedema: adipocyte death and concurrent regeneration. J Cutan Pathol 36: 1293-1298
- Priglinger E et al (2017) The adipose tissue-derived stromal vascular fraction cells from lipedema patients: Are theydifferent? Cytotherapy 19: 849-860
- Prantl L et al (2016) Transcription profile in sporadic multiple symmetric lipomatosis reveals differential expression at the level of adipose tissue-derived stem cells. Plast Reconstr Surg 137: 1181-1190
- Bauer AT et al (2019) Adipose stem cells from lipedema and control adipose tissue respond differently to adipogenic stimulation in Vitro. Plast Reconstr Surg 144: 623-632
- Al-Ghadban S et al (2020) Increase in leptin and PPAR-gamma gene expression in lipedema adipocytes differentiated in vitro from adipose-derived stem cells. Cells 9(2): 430
- Fife CE et al (2010) Lipedema: a frequently misdiagnosed and misunderstood fatty deposition syndrome. Adv Skin Wound Care 23: 81-92
- Szel E et al (2014) Pathophysiological dilemmas of lipedema. Med Hypotheses 83: 599-606
- Poojari A et al (2022) Lipedema: Insights into morphology, pathophysiology, and challenges. Biomedicines 10(12): 3081
- Aksoy H et al (2021) Cause and management of lipedema-associated pain. Dermatol Ther 34(1): 1396-0296
- Kruppa P et al (2020) Lipödem – Pathogenese, Diagnostik und Behandlungsoptionen. Dtsch Arztebl Int 117: 396-403
- Forner-Cordero I et al (2012) Lipedema: an overview of its clinical manifestations, diagnosis and treatment of the disproportional fatty deposition syndrome – systematic review. Clin Obes 2(3-4): 86–95
- Buck DW et al (2016) Lipedema: A relatively common disease with extremely common misconceptions. Plast Reconstr Surg Glob Open 4(9): e1043
- Wollina U et al (2018) Differenzialdiagnostik von Lipödem und Lymphödem: Ein Leitfaden für die Praxis. Z Rheumatol 77(9): 799-807
- Buso G et al (2019) Lipedema: A Call to Action! Obesity (Silver Spring) 27: 1567-1576
- Schleip R et al (2014) Faszien und ihre Bedeutung für die Interozeption. Osteopathische Medizin 15: 25-30
- Michalak J et al (2022) Myofascial Tissue and Depression Cognit Ther Res 46: 560-572
- Child AH et al (2010) Lipedema: an inherited condition. Am J Med Genet A 152a: 970-976
- Torre YS et al (2018) Lipedema: friend and foe. Horm Mol Biol Clin Investig 33(1): /j/hmbci.2018.33.issue-1/hmbci-2017-0076/hmbci-2017-0076.xml
- Verde L et al (2023) Ketogenic diet: a nutritional therapeutic tool for lipedema? Curr Obes Rep 12(4): 529-543
- Di Renzo L et al (2023) Modified mediterranean-ketogenic diet and carboxytherapy as personalized therapeutic strategies in lipedema: a pilot study. Nutrients 15(16): 3654
- Jeziorek M et al (2023) The effect of a low-carbohydrate high-fat diet on laboratory parameters in women with lipedema in comparison to overweight/ obese women. Nutrients 15(11): 2619
- Langendoen SI et al (2009) Lipoedema: from clinical presentation to therapy. A review of the literature. Br J Dermatol 161: 980-986
- Seidel G et al (2019) Selbstmanagement bei chronischen Erkrankungen. In: Nomos Verlagsgesellschaft mbH & Co. KG, Baden-Baden
- Mendoza E (2020) Beitrag als Diskussionsgrundlage zum Thema: Fehlinformation im Internet und Konsequenzen für Patienten und uns Ärzte im täglichen Arbeitsfeld am Beispiel des Lipödems. Phlebologie 49:115-116
- Bodenheimer T et al (2002) Patient self-management of chronic disease in primary care. JAMA 288:2469-2475
- Miller WR et al (2015) Motivierende Gesprächsführung. 3rd edn. Lambertus-Verlag, Freiburg im Breisgau
- Baumgartner A et al (2021) Improvements in patients with lipedema 4, 8 and 12 years after liposuction. Phlebology 36(2): 152-159
- Kruppa P et al (2022) A 10-year retrospective before-and-after study of lipedema surgery: patient-reported lipedemaassociated symptom improvement after multistage liposuction. Plast Reconstr Surg 149(3): 529e-541e
- Wright T et al (2023) Lipedema reduction surgery improves pain, mobility, physical function, and quality of life: case series report. Plast Reconstr Surg Glob Open 11(11): e5436
- Kodim A et al (2023) Mikrokannuläre Liposuktion in Tumeszenzanästhesie beim Lipödem: Eine Analyse von 519 Liposuktionen. Wien Med Wochenschr 173(11-12): 290-298
Bildquellen
Titelbild: © Tatiana – stock.adobe.com
Abb. 2: A. Miller



Tutorielle Unterstützung
Die tutorielle Unterstützung der Fortbildungsteilnehmer erfolgt durch unseren ärztlichen Leiter Dr. med. Alexander Voigt in Zusammenarbeit mit der arztCME-Redaktion. Inhaltliche Fragen können über das Kommentarfeld, direkt per Mail an service@arztcme.de oder via Telefon unter Tel.: +49(0)180-3000759 gestellt werden. Inhaltliche Fragen werden von unserem ärztlichen Leiter bzw. nach Rücksprache mit diesem und evtl. dem Autor auch von der arztCME-Redaktion beantwortet.
Technischer Support
Der technische Support der arztCME-Online-Akademie erfolgt durch geschulte Mitarbeiterinnen und Mitarbeiter des Betreibers health&media GmbH unter der E-Mail-Adresse technik@arztcme.de oder via Telefon unter Tel.: 49(0)180-3000759.